우리가 일상에서 흔히 접하는 알코올에는 여러 가지가 있죠.
소독용 알코올 (에탄올), 인체에 해로운 메탄올, 소주나 맥주 등에 들어있는 에탄올 등 우리 주변에는 다양한 알코올이 있습니다.
지금부터 알코올의 정의, 차수, 성질, IUPAC 명명법을 알려드리겠습니다.
알코올의 정의
Alcohol은 하이드록시기 (hydroxy, -OH)라는 산화수소가 결합된 탄화수소물이다.
알코올의 차수 (classification of alcohol)
알코올에 결합된 알킬기 (R)의 수에 따라 0차, 1차 (primary), 2차 (seconday), 3차 (tertiary) 알코올로 분류한다.
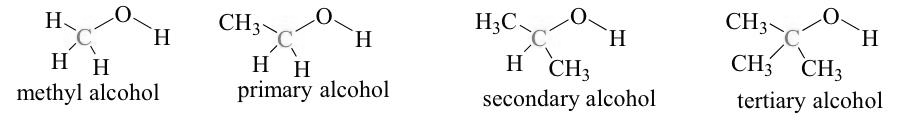
왼쪽부터 순서대로 0차 알코올, 1° 알코올, 2° 알코올, 3° 알코올 순이다.
3차 알코올은 있는데 4차 알코올이 없는 이유는 무엇일까?
- 탄소 원자는 최대 4개의 원자와 결합할 수 있는데 알코올은 이미 한 개의 하이드록시기와 결합을 하고 있는 상태이기 때문에 최대 3개의 알킬기와 결합할 수 있으므로, 3차 알코올까지만 형성이 된다.
0차 알코올은 무엇인가?
- 0차 알코올은 탄소에 알킬기 (R)이 결합하지 않은 상태이며, 0차 알코올에는 methyl alcohol (= methanol)이 있다.
차수에 따라 산화가 다르게 일어나는데, 산화를 하면서 알코올이 알데하이드 (aldehyde), 카복실산 (carboxylic acid), 케톤 (ketone) 등으로 다양하게 변형된다.
알코올의 성질 (physical properties of alcohols)
극성 (polarity):
- 탄화수소 (CH)는 극성을 띄지 않지만, 하이드록시기 (OH)는 극성을 띄기 때문에 알코올은 전체적으로 극성을 띤다.
끓는점 (boiling point):
- 하이드록시기에 있는 수소결합 (hydrogen bonding)이 끓는점을 증가하는 데 기여한다. 또한, 탄소가 많이 결합되어 있을수록 분자를 분리하기 어려워지기 때문에 끓는점이 증가한다고 볼 수 있다.
물에 녹는 성질 (solubility in water):
- 하이드록시기 (OH)는 친수성 (물에 친화성을 나타냄; hydrophilic)을 띄기 때문에 물에 쉽게 녹지만 탄소 원자는 소수성 (물을 싫어함; hydrophobic)을 가지고 있어서 탄소가 1~3개 일 때까지만 물에 녹는다.
(탄소가 3개보다 많은 분자는 탄소의 성질이 더 우세하기 때문에 물에 녹지 않는다.)
산도 (acidity):
- 하이드록시기는 매우 약한 산성 (Bronsted acid)을 띄고, 물보다 약한 산도를 가지고 있다. 알코올의 pKa는 15~20 정도 된다.
산도가 높은 순으로 나열하자면, 물 (H2O) - 메탄올 (CH3OH) - 에탄올 (CH3CH3OH) - 아이소프로판올 (isopropanol; (CH3)2CHOH) - tert-부틸알코올 (tert-butanol; (CH3)3COH) 순이다.
알코올 명명법 (IUPAC)
[IUPAC 명명법]
*IUPAC은 International Union of Pure and Applied Chemistry를 줄인 말로, 국제순수/응용화학연합을 뜻한다.
알케인 (alkane) 뒤에 붙은 'e'를 빼고 'ol'을 붙이면 된다.
예를 들어 메테인 (methane)은 메탄올 (methanol)이 된다.
| 알케인 명명 / 화학식 | 알코올 명명 / 화학식 | Common name (통상적 이름) | Classification (차수) |
| methane / CH4 | methanol / CH3OH | methyl alcohol | 0차 |
| ethane / CH3CH3 or C2H6 | ethanol / CH3CH2OH | ethyl alcohol | 1차 |
| propane / C3H8 | propanol / C3H7OH | propyl alcohol | 1차 |
| butane / C4H10 | butanol / C4H9OH | buthyl alcohol | 1차 |
하이드록실기의 위치를 표시해야 하는 경우 (-OH가 몇 번째 탄소에 붙어있는지) 2가지 방법이 있다.
- 하이드록실기 위치를 '-ol' 바로 전에 표기하는 법
- 하이드록실기 위치를 먼저 표기하는 법
- 2번의 경우, 치환기를 명명한 뒤 붙임표 (hyphen)를 사용해서 하이드록실기의 위치를 표기하고 '-ol'을 적어준다.
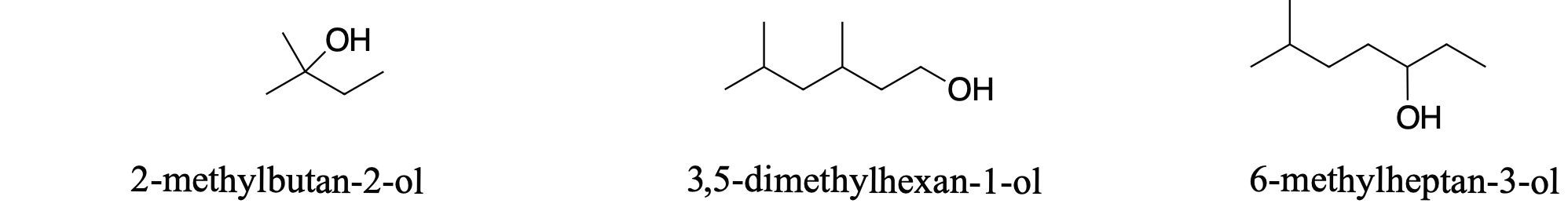
ex. 1번의 경우로 명명할 경우, 아래 그림에 나오는 첫번째 화합물은 "2-methylbutan-2-ol"이다.
똑같은 화합물을 2번의 경우로 명명할 경우에는, "2-methyl-2-butanol"이 된다.
이와 같이 아래의 화합물들은 2가지 방식으로 명명할 수 있다.
| 1번 방식으로 명명 | 2번 방식으로 명명 |
| 2-methylbutan-2-ol | 2-methy-2-butanol |
| 3,5-dimethylhexan-1-ol | 3,5-dimethyl-1-hexanol |
| 6-methylheptan-3-ol | 6-methyl-3-heptanol |
[Common name / 통상적 명명]
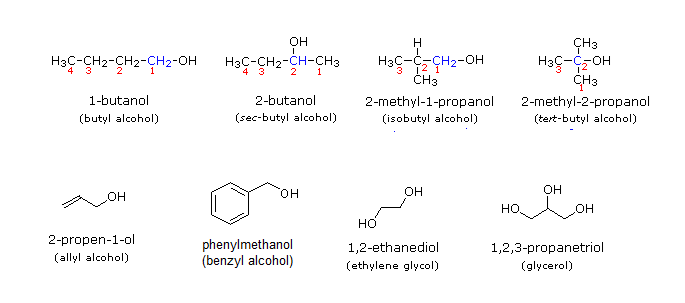
통상적으로는 치환기 이름 + '알코올'을 붙여서 명명합니다. IUPAC 명명법과는 다르지만 일상에서 많이 쓰이고 친숙한 이름들이니 익혀두는 게 좋아요!
'미국대학공부' 카테고리의 다른 글
| [화학통계분석] 정확성와 정밀도 (0) | 2023.03.08 |
|---|